随着2021年医疗器械注册人制度的全面实施,医疗器械跨区域委托生产逐渐成为常态,在极大促进产业发展的同时也带来了跨区域监管难题。浙江省药监局聚焦监管痛点,带领绍兴市市场监管局创新开发“医疗器械跨区域监管平台”,以数字化手段推动线上线下一体化治理,促进各地监管责任落实,实现跨区域协同高效检查,服务全国统一大市场建设。
随着2021年医疗器械注册人制度的全面实施,医疗器械跨区域委托生产逐渐成为常态,在极大促进产业发展的同时也带来了跨区域监管难题。浙江省药监局聚焦监管痛点,带领绍兴市市场监管局创新开发“医疗器械跨区域监管平台”,以数字化手段推动线上线下一体化治理,促进各地监管责任落实,实现跨区域协同高效检查,服务全国统一大市场建设。
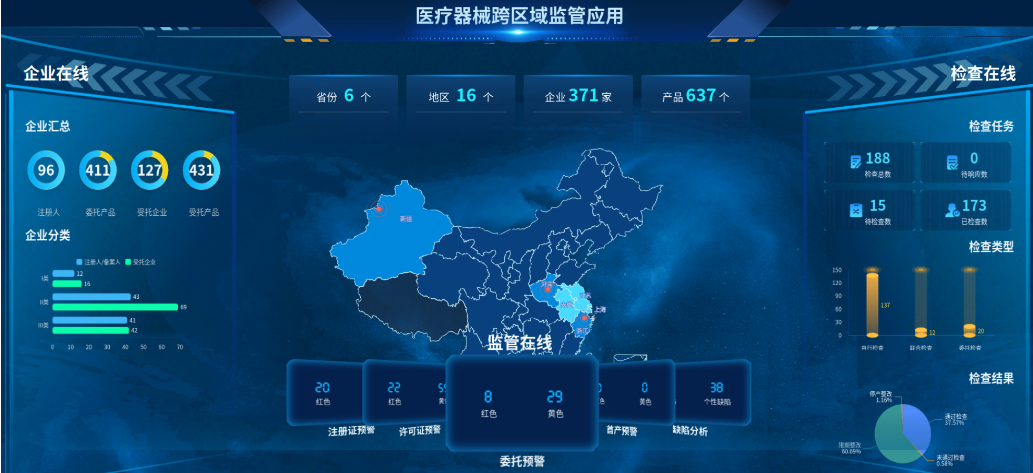
一是畅通跨省数据互联渠道。针对医疗器械跨省关联企业海量数据互联互通难题,平台通过集成化数据打包,建立数据信息库,归集主体登记、产品质量、行政处罚、不合格报告、不良事件监测等信息数据,向属地监管部门开放数据端口,有效打破数据流通壁垒,为属地监管部门掌握企业全貌提供数据支撑,实现“数据跑”代替“人工跑”。截至目前,平台归集上海、江苏、浙江、安徽、河南、新疆等6省(自治区、直辖市)医疗器械注册申请人信息209家、受托生产企业信息184家,包含委托生产产品418件、受托生产产品437件。

二是打造跨省报告互认模式。监管标准不统一、检查报告不互认是实现跨区域监管的核心难题。平台以开放数据端口为基础,科学设置报告上传、共享查询、数据统计等功能,确保不同区域的监管人员能实时上传、查阅、统计相关医疗器械企业的检查报告。同时,通过配置后台权限,系统可根据检查人员的实际需求设置共享权限,有效保护企业数据安全。截至目前,通过联合检查、委托检查、自行检查,形成检查报告174份,涉及企业100余家。
三是探索跨省检查队伍建设。2021年,浙江绍兴联合新疆博州、河南许昌成立全国首个医疗器械跨区域监管联盟,组建首支医疗器械跨区域监管检查员队伍。2024年,随着上海、江苏、浙江、安徽、河南、新疆等“6省先试”,医疗器械跨区域监管检查员队伍已成长为一支242人、包含6省(自治区、直辖市)医疗器械监管业务骨干的高素质检查员队伍,并在不断协同合作中形成了信息互通、人员互派、结果互认的“三互”机制,医疗器械跨区域监管效能持续深化。
下一步,浙江省药监局将按照国家药监局工作要求,继续深化跨区域监管模式探索,推动数据流动“横向”跨区域、“纵向”跨层级,持续扩大应用使用领域和覆盖面,让实践成果在更大范围共享,为促进医疗器械行业高质量发展提供坚实数字底座。